北理工課題組在人工智能新藥研發(fā)中取得重要進展
發(fā)布日期:2025-07-02 供稿:化學(xué)與化工學(xué)院 攝影:化學(xué)與化工學(xué)院
編輯:田柳 審核:王振華 閱讀次數(shù):
2025年7月1日,北京理工大學(xué)化學(xué)與化工學(xué)院于明加副研究員和梁建華教授與物理學(xué)院蔣偉教授團隊在國際頂級期刊Journal of Agricultural and Food Chemistry發(fā)表題為“AI-Accelerated Identification of Novel Antimicrobial Peptides for Inhibiting Fusarium graminearum ”的研究論文(DOI: 10.1021/acs.jafc.5c03429)。
該團隊在針對禾谷鐮刀菌( Fusarium graminearum )引起小麥赤霉病造成的糧食減產(chǎn)和毒素中毒等環(huán)境安全和生命健康等問題,通過人工智能模型與計算物理方法加速設(shè)計出新型抗菌肽TP,僅需13.33微摩爾濃度即可近乎完全殺滅病原真菌禾谷鐮刀菌。這項AI與化學(xué)的交叉研究為保障全球糧食安全提供了新的思路。
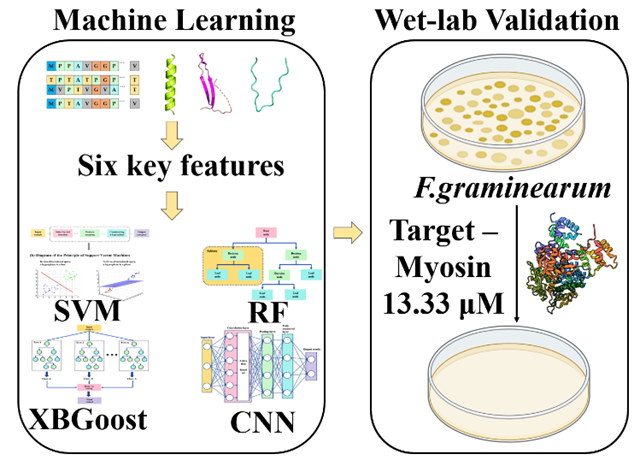
圖1. 研究摘要。
研究團隊創(chuàng)新構(gòu)建了抗菌肽人工智能設(shè)計平臺。通過建立較大規(guī)模的抗菌肽數(shù)據(jù)庫,并精準鎖定六項關(guān)鍵理化特征,成功建立四大預(yù)測模型。其中XGBoost模型表現(xiàn)最為卓越(預(yù)測精度R2=0.77),猶如裝上"分子雷達"般高效篩查有效肽段。通過該模型設(shè)計的六肽TP(KGPPRR)在實驗中展現(xiàn)出驚人效力——僅需微量濃度即可完全抑制病原菌生長。
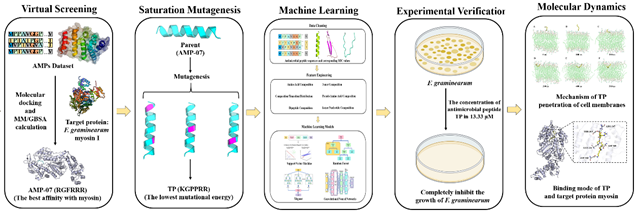
圖2. 研究的流程。
分子動力學(xué)模擬首次揭示其雙重作用機制:肽鏈先通過靜電作用錨定真菌細胞膜,隨后通過疏水性插入穿透屏障,最終精準結(jié)合致病關(guān)鍵靶點肌球蛋白,阻斷病菌ATP水解。這種結(jié)合使病原菌喪失營養(yǎng)運輸能力,如同被切斷"細胞生命線"。特別值得注意的是,該肽段靶向的肌球蛋白恰是當前主流殺菌劑的薄弱環(huán)節(jié),為解決日益嚴峻的耐藥性問題提供新策略。
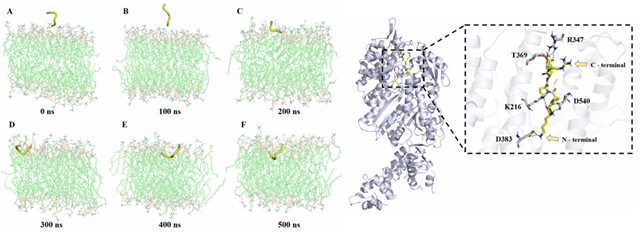
圖3. 抗菌肽TP的穿膜機制和與靶蛋白的結(jié)合模式。
與傳統(tǒng)農(nóng)藥研發(fā)相比,這項AI驅(qū)動技術(shù)縮短開發(fā)周期縮短,降低成本。該成果不僅創(chuàng)下單肽抗菌效率新紀錄,更開創(chuàng)了"計算機設(shè)計-實驗驗證-機理解析"的智能農(nóng)藥研發(fā)新模式,為全球糧食安全鑄造"數(shù)字防護盾"。
本研究受到國家自然科學(xué)基金青年科學(xué)基金(32201053)、北京理工大學(xué)青年教師學(xué)術(shù)啟動計劃(3100012222222)資助。
文章鏈接:https://pubs.acs.org/doi/10.1021/acs.jafc.5c03429
附作者簡介:
共同第一作者:冉躍,北京理工大學(xué)化學(xué)與化工學(xué)院碩士生。
共同第一作者:李森,北京理工大學(xué)化學(xué)與化工學(xué)院博士生。
通訊作者:于明加,北京理工大學(xué)副研究員,主要從事智能藥物設(shè)計算法開發(fā)以及重大疾病相關(guān)的新藥創(chuàng)制。梁建華,北京理工大學(xué)教授,主要從事藥物化學(xué)和新藥創(chuàng)制研究。蔣偉,北京理工大學(xué)教授,主要從事計算物理和自旋電子學(xué)研究。
分享到:
