北理工團隊在光激活外泌體增敏腫瘤免疫治療方面取得重要進展
發(fā)布日期:2022-09-17 供稿:前沿交叉科學研究院
編輯:朱倩云 審核:唐水源 閱讀次數(shù):
近日,國際頂級期刊Advanced Materials(影響因子32.086)報道了北京理工大學黃淵余課題組在光激活外泌體增敏腫瘤免疫治療方面的研究進展,相關(guān)成果以“Photoactivatable Silencing Extracellular Vesicle (PASEV) Sensitizes Cancer Immunotherapy”為題發(fā)表。該工作第一作者為北京理工大學前沿交叉科學研究院/生命學院博士后陸梅博士、國家納米科學中心邢昊楠博士,通訊作者為國家納米科學中心梁興杰研究員(北理工兼職教授)、北理工黃淵余教授,北理工為論文第一單位。
臨床上患者對單一免疫療法的總體響應(yīng)率僅為10-30%。如何提高患者響應(yīng)率是腫瘤免疫治療領(lǐng)域有待攻克的重點。最近研究發(fā)現(xiàn),P21活化激酶4(p21-activated kinase 4,PAK4)是腫瘤阻止殺傷性T細胞浸潤,實現(xiàn)免疫逃逸的關(guān)鍵靶點。在低T細胞浸潤患者的腫瘤組織中,PAK4表達豐富。此外,免疫原性弱也是導(dǎo)致腫瘤免疫治療耐受的重要因素。胞外囊泡是新一代的藥物遞送載體,近年來廣泛用于siRNA等核酸藥物的遞送,具低免疫原性、良好的循環(huán)穩(wěn)定性及腫瘤趨向性。
基于此,梁興杰研究員與黃淵余教授團隊設(shè)計了新型的光激活胞外囊泡(PASEV),將免疫浸潤與免疫激活進行有機組合,協(xié)同增敏腫瘤免疫治療。首先,針對腫瘤阻止免疫細胞浸潤、實現(xiàn)免疫逃逸的關(guān)鍵靶點PAK4,設(shè)計可特異沉默PAK4表達的siRNA(siPAK4),并將其與光可激活、活性氧(ROS)敏感的聚乙烯亞胺(PEI)進行組裝,形成納米復(fù)合物。然后,用M1型巨噬細胞的胞外囊泡對納米復(fù)合物核心進行偽裝,賦予其良好的生物相容性、良好的循環(huán)穩(wěn)定性及腫瘤趨向性(圖1)。
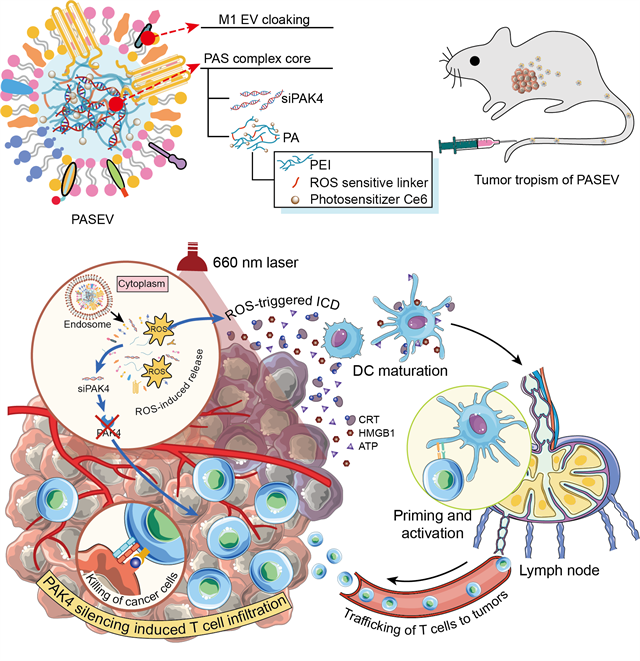
圖1 PASEV的制備及抗腫瘤機制示意圖
作者闡明了光激活胞外囊泡增敏腫瘤免疫治療的機制,siPAK4可從源頭上有效沉默腫瘤“守衛(wèi)兵”PAK4的表達,阻斷WNT/β-catenin信號通路,增加腫瘤組織中趨化因子CCL4等的表達水平,從而將細胞毒性T淋巴細胞招募到腫瘤內(nèi)部,浸潤腫瘤組織;光激活聚合物材料則可通過免疫原性細胞死亡級聯(lián)反應(yīng)(ICD)增強腫瘤免疫原性,促進樹突細胞成熟,激活細胞毒性CD8+ T細胞(圖2)。該研究為提高當前腫瘤免疫治療的響應(yīng)率,實現(xiàn)免疫增敏提供了新思路。
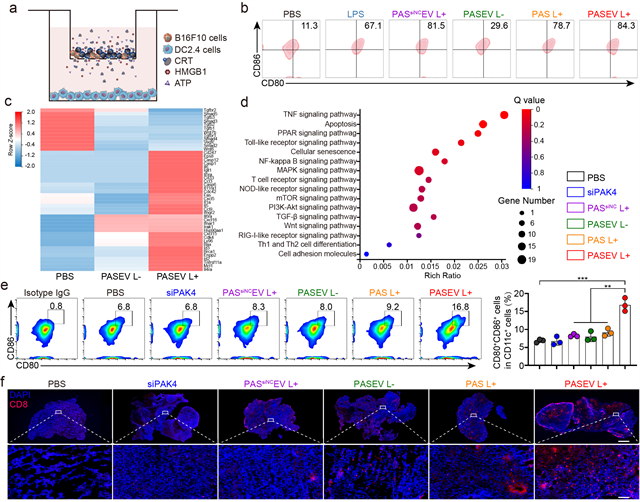
圖2 PASEV增敏腫瘤免疫治療的機制
論文鏈接: https://doi.org/10.1002/adma.202204765
分享到:
