北理工在“簇發(fā)光”螺環(huán)聚合物用于腫瘤細胞識別與診斷取得研究成果
發(fā)布日期:2020-02-25 供稿:材料學(xué)院 蔡政旭
編輯:邵澤 審核:金海波 閱讀次數(shù):P53是一種腫瘤抑制蛋白,它可以控制受到損傷的DNA進行修復(fù)或使受損傷較大的細胞進入凋亡過程,避免其在不利條件下無限分裂。在腫瘤細胞中,p53的表達和活性往往受到高表達的MDM2蛋白抑制,其機理是p53可以插入MDM2蛋白的Trp26,Phe19和Leu26疏水腔中,并與其緊密結(jié)合,從而生理活性受到限制。
近日,在國家自然科學(xué)基金重大項目(批準號:21490574)和面上項目(批準號:21474009和51673024)資助下,北京理工大學(xué)董宇平課題組與韓國高麗大學(xué)Kim Jong Seung課題組合作,報道了利用腫瘤細胞中高表達的MDM2蛋白與非傳統(tǒng)共軛的螺環(huán)聚合物結(jié)合,在產(chǎn)生“簇”發(fā)光的同時,限制p53與MDM2蛋白結(jié)合,從而釋放并活化p53蛋白,促進了癌細胞凋亡,實現(xiàn)對腫瘤細胞靶向診斷和治療的相關(guān)工作。
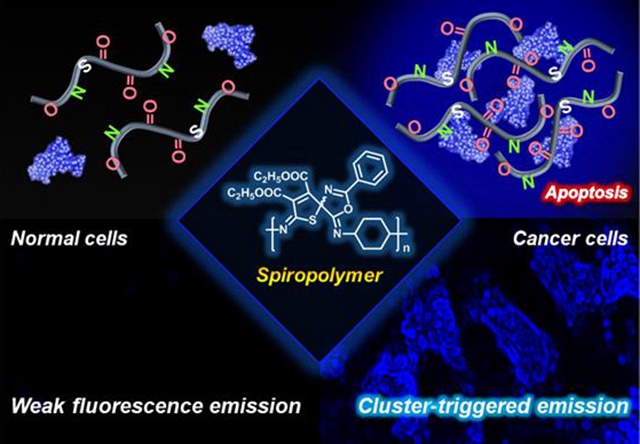
螺環(huán)化合物因其獨特的化學(xué)結(jié)構(gòu),具有良好的生物活性和穩(wěn)定性,目前已被用于多種藥物中,如依尼螺酮、丁螺環(huán)酮等,但螺環(huán)聚合物的合成與應(yīng)用卻少見報道。本成果首先利用“無催化、一步法”三鍵聚合反應(yīng)合成了新型螺環(huán)聚合物。實驗結(jié)果表明該螺環(huán)聚合物具有典型的簇發(fā)光(Cluster Triggered Emission, CTE)特性。體外條件下,MDM2蛋白可以與螺環(huán)聚合物發(fā)生相互作用,誘導(dǎo)P1a2b進一步聚集而引發(fā)簇發(fā)光;因此在MDM2高表達的多種腫瘤細胞中均呈現(xiàn)明顯的藍色熒光,然而在MDM2蛋白低表達的正常細胞則無明顯發(fā)光,能夠?qū)崿F(xiàn)對正常細胞和腫瘤細胞的有效區(qū)分,并且高分子量P1a2b成像效果更為明顯。作者通過MDM2的抑制劑Nutlin-3與P1a2b的競爭實驗驗證細胞內(nèi)P1a2b螺環(huán)聚合物的作用位點,發(fā)現(xiàn)P1a2b與Nutlin-3混合后的MDM2蛋白和細胞相互作用,均不能表現(xiàn)簇發(fā)光特性,表明Nutlin-3優(yōu)先占據(jù)了MDM2蛋白的作用位點,使P1a2b不能與之有效結(jié)合,進而不能引發(fā)聚合物簇聚集發(fā)光。
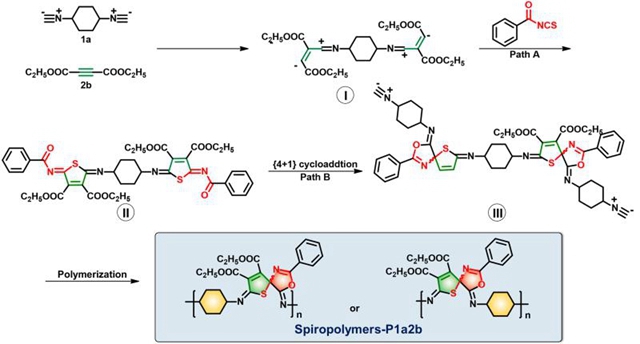
圖1 螺環(huán)聚合物的合成路線
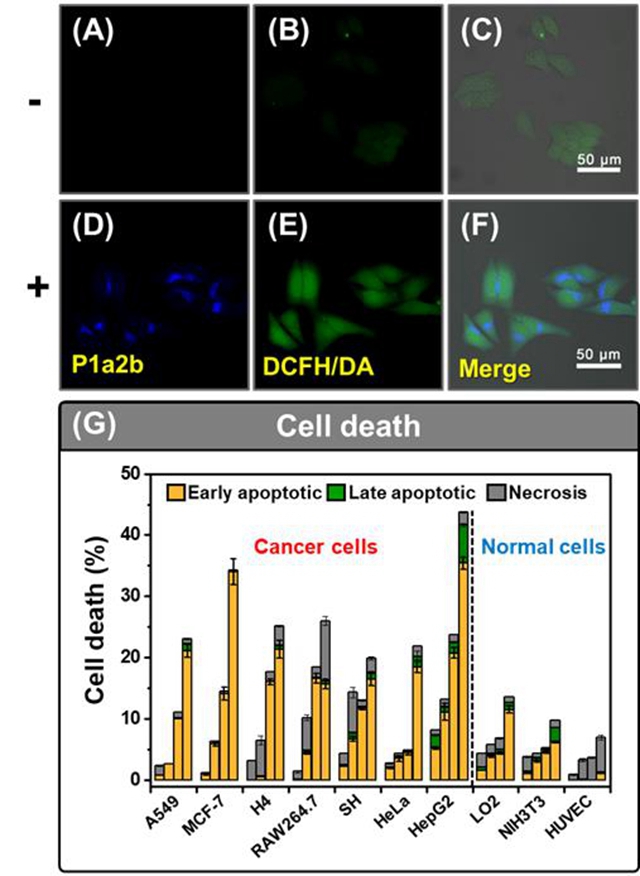
圖2 (A)(B)(C) 未加P1a2b聚合物的DAPI,F(xiàn)ITC場與合并照片;(D)(E)(F) 加入P1a2b聚合物的DAPI,F(xiàn)ITC場與合并照片;(G) 與P1a2b聚合物共培養(yǎng)24 h, 48 h, 72 h后的細胞凋亡率。
隨后,作者利用蛋白質(zhì)免疫印跡法(Western blot)證實了經(jīng)過P1a2b共培養(yǎng)細胞中的p53蛋白的表達增加。同時證明了P1a2b加入后,p53的增加會導(dǎo)致其相關(guān)的ROS濃度的增長,解釋了P1a2b聚合物誘使腫瘤細胞高凋亡的主要原因。同時,作者利用分子對接軟件,將P1a2b的三聚體與MDM2蛋白計算,證實其與Trp26,Phe19和Leu26疏水空腔結(jié)合,且結(jié)合穩(wěn)定。
鑒于該螺環(huán)聚合物合成簡單,具備腫瘤細胞靶向診斷與治療相結(jié)合的能力,為新型螺環(huán)聚合物應(yīng)用提供了新思路,為腫瘤的治療和診斷提供了新方法。劉派和付偉強博士為此工作共同第一作者,蔡政旭特聘研究員、董宇平教授、Kim Jong Seung教授為此工作通訊作者。
這一成果近期發(fā)表在Angewandte Chemie International Edition上,原文鏈接為: https://onlinelibrary.wiley.com/doi/10.1002/anie.201916524。
分享到:
