北理工團(tuán)隊在小干擾核酸藥物方面取得研究成果
發(fā)布日期:2022-09-14 供稿:前沿交叉科學(xué)研究院
編輯:朱倩云 審核:唐水源 閱讀次數(shù):近日,北京理工大學(xué)前沿交叉科學(xué)研究院黃淵余課題組在國際頂級期刊《Trends in Molecular Medicine》(影響因子15.272)發(fā)表題為《siRNA modification and delivery for drug development》的“Strategy”論文,文章總結(jié)了幾種代表性的siRNA修飾策略及遞送方式,并對siRNA藥物的優(yōu)勢和挑戰(zhàn)進(jìn)行了討論。論文通訊作者為北京理工大學(xué)黃淵余教授,第一作者為北京理工大學(xué)生命學(xué)院/前沿交叉科學(xué)研究院博士生張萌潔。
小干擾RNA(small interfering RNA,siRNA)是一類長度約為20-25個核苷酸的雙鏈RNA分子,其通過曾獲得諾貝爾獎的RNA干擾機(jī)制抑制靶基因的表達(dá),即siRNA反義鏈通過堿基互補配對原則與靶mRNA結(jié)合、介導(dǎo)mRNA的剪切,從而阻止靶mRNA翻譯成蛋白質(zhì)。siRNA因其理論上能抑制任意基因的表達(dá)而成為基礎(chǔ)研究與制藥應(yīng)用的熱點。截止目前,全球已有5款siRNA藥物獲批上市,且制藥技術(shù)已實現(xiàn)單次給藥后藥效持續(xù)一年、甚至一年以上,此為人類制藥歷史的革命性進(jìn)步。
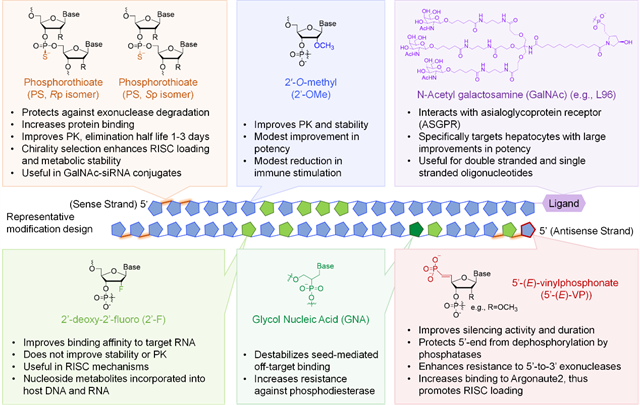
圖1.常用的siRNA化學(xué)修飾單體及其功能特點
siRNA制藥需要解決siRNA分子不夠穩(wěn)定、可能產(chǎn)生脫靶效應(yīng)、以及需要開發(fā)安全高效的遞送系統(tǒng)等關(guān)鍵問題。該論文首先以代表性的siRNA化學(xué)修飾方案為例,概述了常用的化學(xué)修飾單體,包括硫代磷酸骨架修飾、甲氧基修飾、氟代修飾、GNA修飾、5’-(E)-VP修飾等,并對每種化學(xué)修飾方式的作用機(jī)制或功能特點進(jìn)行了凝練總結(jié)。各種修飾單體的作用相輔相成,有效地增強了siRNA的穩(wěn)定性、消除/降低了脫靶效應(yīng)和免疫原性,顯著提高了成藥性,GalNAc-siRNA綴合則實現(xiàn)了高效的肝實質(zhì)細(xì)胞靶向遞送。
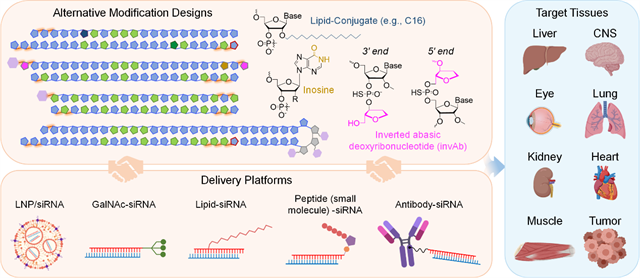
圖2. 其它修飾策略及多種siRNA遞送技術(shù)
論文進(jìn)一步提供了其它幾種代表性的siRNA修飾模式,給出了siRNA遞送的代表性研究方向。文章提到,目前已獲批上市的5種siRNA藥物是通過脂質(zhì)納米顆粒(LNP)和GalNAc綴合實現(xiàn)肝靶向遞送和疾病治療;在后續(xù)的研究開發(fā)中,可通過其它遞送方式將siRNA遞送到中樞神經(jīng)系統(tǒng)、眼睛、肺臟、腎臟等非肝組織,進(jìn)而建立一系列的非肝靶點的藥物開發(fā)平臺。
論文鏈接:https://www.sciencedirect.com/science/article/pii/S1471491422002040
附作者簡介:
張萌潔,北京理工大學(xué)生命學(xué)院/前沿交叉科學(xué)研究院博士生,目前以第一作者在Advanced Science、Trends in Molecular Medicine、Nano Research、ACS Applied Materials & Interfaces期刊發(fā)表論文4篇,發(fā)表英文專著章節(jié)1章,已授權(quán)專利1件。
黃淵余,北京理工大學(xué)前沿交叉科學(xué)研究院教授、博士生導(dǎo)師,國家級青年人才、北京市科技新星、北京市科協(xié)青年托舉人才。研究主要圍繞核酸技術(shù)與藥物/疫苗展開。以通訊/第一作者在Sci Adv、Signal Transduct Target Ther、Adv Mater等發(fā)表論文60余篇,含IF>10的30余篇;共發(fā)表論文90余篇,撰寫10余部專著章節(jié),申請18件專利,含PCT專利3件。作為課題負(fù)責(zé)人或主持人先后承擔(dān)國家重點研發(fā)計劃、國家自然科學(xué)基金等項目10余項,獲得北京市科學(xué)技術(shù)獎自然科學(xué)一等獎(排名第九)、廣西科學(xué)技術(shù)獎自然科學(xué)一等獎(排名第五)、中美納米醫(yī)學(xué)與納米生物技術(shù)學(xué)會“未來之星”獎等榮譽。是中國生物物理學(xué)會納米生物學(xué)分會秘書長,多個學(xué)會理事或委員;是Exploration創(chuàng)刊副主編(Wiley出版)、多個期刊(青年)編委。
分享到:
