北理工和UIC大學(xué)合作在大環(huán)內(nèi)酯新作用機制發(fā)現(xiàn)方面取得重要進展
發(fā)布日期:2024-07-23 供稿:化學(xué)與化工學(xué)院 攝影:化學(xué)與化工學(xué)院
編輯:田柳 審核:王振華 閱讀次數(shù):
近日,北京理工大學(xué)化學(xué)與化工學(xué)院梁建華教授與美國伊利諾伊大學(xué)芝加哥分校核糖體生化專家Alexander S. Mankin教授和核糖體晶體結(jié)構(gòu)學(xué)家Yury S. Polikanov副教授合作,在設(shè)計不同作用機制的抗耐藥菌大環(huán)內(nèi)酯取得重要進展。相關(guān)成果以“Macrolones target bacterial ribosomes and DNA gyrase and can evade resistance mechanisms”為題發(fā)表于國際頂刊《Nature Chemical Biology》。通訊單位是伊利諾伊大學(xué)芝加哥分校和北京理工大學(xué),伊利諾伊大學(xué)芝加哥分校的Elena V. Aleksandrova, 北京理工大學(xué)化學(xué)與化工學(xué)院的博士生馬聰璇和伊利諾伊大學(xué)芝加哥分校的Dorota Klepacki為共同第一作者,梁建華教授,Yury S. Polikanov副教授和Alexander S. Mankin教授為共同通訊作者。
目前臨床半數(shù)抗生素作用于核糖體,核糖體的結(jié)構(gòu)非常龐大和復(fù)雜,其結(jié)構(gòu)和功能的解析在2000年左右取得突破,三位研究者萬卡特拉曼-萊馬克里斯南、托馬斯-施泰茨和阿達-尤納斯因此獲得2009年諾貝爾化學(xué)獎。大環(huán)內(nèi)酯類藥物如紅霉素、克拉霉素、阿奇霉素等因為其副作用少,安全性高被廣泛用于上下呼吸道細菌性感染的治療。然而抗生素的長期使用以及細菌的進化使得細菌耐藥性日益嚴重,其中erm耐藥基因表達的甲基化酶會導(dǎo)致骨架迥異的大環(huán)內(nèi)酯類、林可酰胺類和鏈陽菌素B類的共同抗菌作用位點即核糖體A2058被甲基化修飾,這類交叉耐藥性被稱作MLSB類耐藥。為了得到能夠抗耐藥菌且減緩細菌耐藥突變的抗生素,使用藥效團融合策略將大環(huán)內(nèi)酯與喹諾酮連接得到的雜合物——“macrolone”有可能突破目前的MLSB類耐藥,然而當(dāng)前研究存在的局限性是:一方面目前其他課題組報道的大環(huán)內(nèi)酯和喹諾酮的雜合物不具有雙靶標模式,仍然只作用于核糖體;另一方面目前已知的抗耐藥菌靶點為核糖體堿基A752-U2609,代表性上市藥物是泰利霉素,但是其抗高水平耐藥菌仍有很大不足,目前其他同質(zhì)性抗生素未能獲得上市批準,亟需針對耐藥機制尋找新的核糖體作用位點。
近十余年來,梁建華團隊在抗耐藥菌大環(huán)內(nèi)酯上不斷迭代設(shè)計,從數(shù)百種抗耐藥菌大環(huán)內(nèi)酯中挑選了3種代表性的“macrolone”結(jié)構(gòu),與Yury S. Polikanov副教授和Alexander S. Mankin教授合作進行了機制研究。通過體內(nèi)雙基因報告(圖a)和體外蛋白翻譯轉(zhuǎn)錄抑制實驗以及DNA超螺旋抑制實驗確定三種結(jié)構(gòu)的主要作用靶標是不同的,分別是MCX-91主要作用于核糖體、MCX-66主要作用于DNA促旋酶、MCX-128能夠同時作用于核糖體以及DNA促旋酶。模式菌 Thermus thermophilus 核糖體與這三個化合物的高分辨率復(fù)合物晶體結(jié)構(gòu)(分辨率是2.35?-2.60?)顯示作用于核糖體的C2586-C1782新位點(圖b),這與我們先前臨床病原菌金黃色葡萄球菌(MRSA)核糖體與化合物MCX-190的復(fù)合物冷凍電鏡結(jié)構(gòu)解析結(jié)果一致(Cell Discovery, 2024, 10(75),DOI : 10.1038/s41421-024-00702-y)。兩種不同的核糖體結(jié)構(gòu)解析技術(shù)相互印證了我們的化合物在不同菌株中均能作用于新位點C2586-C1782;并且MCX-128對于A2058雙甲基化的模式菌核糖體也能夠緊密結(jié)合,證明了其較好的抗耐藥菌的新模式。而后我們又對化合物的抑制蛋白質(zhì)翻譯特征以及是否誘導(dǎo)細菌產(chǎn)生耐藥特性進行了研究,通過toeprinting技術(shù)對化合物抑制蛋白翻譯的停止位點研究發(fā)現(xiàn),傳統(tǒng)紅霉素允許翻譯的肽鏈長度較長,而MCX系列化合物在翻譯較短肽鏈時即可停止(圖c);紅霉素會誘導(dǎo)erm耐藥基因表達,但MCX系列化合物則不會誘導(dǎo)耐藥基因表達,因此MCX系列化合物具有不同于以往大環(huán)內(nèi)酯的新作用模式。特別需要指出的是,化合物MCX-128具有雙靶標作用機制,藥物在使用過程中當(dāng)單一靶標突變時,化合物MCX-128作用另一靶標則能夠有效地抑制單靶標突變的菌株,使其無法幸存下來,因此在MCX-128對抗下細菌很難同時在核糖體以及DNA促旋酶同時發(fā)生自發(fā)突變(圖d),而相比之下單作用機制的化合物MCX-66和MCX-91較容易產(chǎn)生突變菌株。這樣既不容易誘導(dǎo)耐藥基因表達,又不容易使細菌產(chǎn)生自發(fā)突變的藥物在臨床使用具有很大的優(yōu)勢。
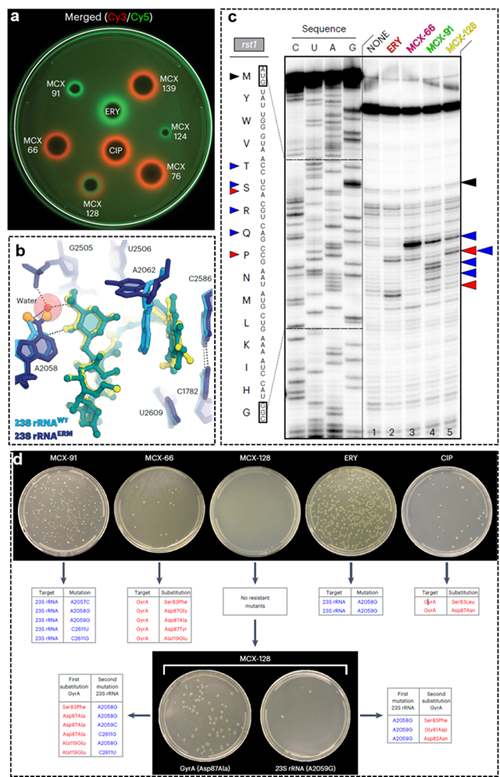
化合物的作用機制
該項研究證實通過合理藥物設(shè)計能夠控制大環(huán)內(nèi)酯與喹諾酮雜合物的主要作用靶標,啟發(fā)人們意識到藥物設(shè)計的新化學(xué)空間。同時,我們基于核糖體的新作用位點創(chuàng)造性地設(shè)計了一個喹諾酮骨架藥效團,使化合物既作用于核糖體新位點又作用于拓撲異構(gòu)酶,一石二鳥。在本研究中,喹諾酮抗生素通過合理設(shè)計再利用,能作為一個藥效團作用于非傳統(tǒng)的核糖體靶標,這極大拓展了經(jīng)典抗生素再應(yīng)用的新思路。
上述研究工作得到了國家自然科學(xué)基金項目、國家研發(fā)重點計劃-合成生物學(xué)專項的支持。
論文信息:https://www.nature.com/articles/s41589-024-01685-3
Elena V. Aleksandrova#, Cong-Xuan Ma#, Dorota Klepacki#, Faezeh Alizadeh, Nora Vázquez-Laslop, Jian-Hua Liang*, Yury S. Polikanov*, Alexander S. Mankin*. Macrolones target bacterial ribosomes and DNA gyrase and can evade resistance mechanisms. Nature Chemical Biology, 2024, DOI: 10.1038/s41589-024-01685-3
附通訊作者簡介:
梁建華,教授,博士生導(dǎo)師,北京市優(yōu)秀人才,新藥創(chuàng)制與綠色合成研究所所長,醫(yī)藥分子科學(xué)與制劑工程工信部重點實驗室副主任。研究方向為藥物化學(xué),致力于治療各種重大疾病的相關(guān)創(chuàng)新藥物開發(fā),研究興趣包括抗耐藥菌抗炎藥物、抗神經(jīng)退行性藥物和抗糖尿病藥物等領(lǐng)域。目前主持參與國家研發(fā)重點計劃項目、科技創(chuàng)新2030重大項目、國家自然科學(xué)基金以及北京市自然科學(xué)基金等課題項目。在Cell Discovery、Eur. J. Med. Chem.、Bioorg. & Med. Chem.、Bioorg. & Med. Chem. Lett.、Curr. Med. Chem.、Curr. Top. Med. Chem.、J. Antibiotics等主流學(xué)術(shù)期刊上發(fā)表通訊作者論文30余篇,第一發(fā)明人授權(quán)中國專利11項、美國專利1項和PCT專利4項。
分享到:
